清华新闻网4月17日电 脑脊液是维持中枢神经系统稳态的重要体液环境,具有机械缓冲、代谢支持、神经发育调控及脑功能维持等多重作用。脉络丛(choroid plexus)作为脑脊液产生与稳态维持的核心结构,暴露于脑脊液流动带来的机械刺激中。然而,对于脉络丛上皮细胞如何感知机械信号,进而调控脑脊液稳态,目前尚缺乏清晰的机制解释。
近期,清华大学药学院肖百龙教授团队研究揭示了机械门控离子通道Piezo1是脉络丛上皮细胞中表达的关键机械信号转导分子,将机械刺激转化为细胞内Ca²⁺信号,进而调控纤毛发生以及脑脊液稳态维持,防止脑积水发生。无论Piezo1功能降低还是过度增强,都会打破这一稳态平衡,导致交通性脑积水(communicating hydrocephalus)发生。该工作不仅拓展了对脉络丛神经生物学功能的认识,也为脑积水这类病因复杂的神经系统疾病提供了新的病理机制启发以及潜在的干预靶点。
研究人员发现机械力受体Piezo1在脉络丛中高表达,且主要定位于成熟脉络丛上皮细胞的顶端膜和侧向细胞连接区域,而在邻近的室管膜细胞中几乎不表达。进一步的膜片钳和Ca²⁺成像实验表明,Piezo1作为机械门控离子通道,能够介导脉络丛上皮细胞对机械力刺激以及化学激动剂Yoda1的响应,并维持细胞内基础Ca²⁺稳态。这些研究结果表明Piezo1作为脉络丛上皮细胞中的关键机械信号转导分子,将机械信号转化为细胞内钙信号。
为了进一步探究Piezo1在体内的功能,研究人员分别利用AAV5-Cre病毒系统和FoxJ1-CreER系统,在小鼠脉络丛上皮细胞中实现了Piezo1的特异性敲除或过表达。一个值得注意的结果是,无论在脉络丛上皮细胞中敲除Piezo1,还是过表达Piezo1,小鼠都会出现明显的脑室扩张和脑积水表型。磁共振成像显示,这些小鼠出现脑室扩大和脑脊液过度积累。进一步通过脑室染料示踪实验,研究人员发现这种脑积水并非由导水管或脑室系统阻塞引起,而更符合交通性脑积水的特征。与之相一致,脑脊液示踪实验还表明,无论Piezo1功能下降还是增强,都会导致脑脊液排出效率下降。
这一结果提示,Piezo1在脉络丛中并不是“越强越好”或“越弱越好”,而是需要维持在一个合适的稳态范围内。过低或过高的机械转导活动,都会打破Piezo1所介导的脑脊液系统的动态平衡。
研究人员对脉络丛上皮细胞进行了转录组分析,结果发现,在Piezo1敲除和过表达两种条件下,均有一批共同下调的基因显著富集于纤毛发生、轴丝组装和纤毛运动等相关通路。进一步的组织染色证实,这些小鼠的脉络丛上皮细胞均出现纤毛数量减少、纤毛长度缩短等显著缺陷。更进一步,研究人员在原代培养的脉络丛上皮细胞中证明,Piezo1通过调控细胞内Ca²⁺稳态来影响纤毛形成与维持。Piezo1缺失会降低基础Ca²⁺水平,而Piezo1过表达则导致Ca²⁺信号过强;两种失衡状态都会破坏纤毛稳态。药理学实验进一步表明,适度调节Ca²⁺信号可以部分恢复由Piezo1异常引起的纤毛缺陷。
这些结果共同表明,Piezo1通过维持一个适宜的Ca²⁺稳态范围,精细控制脉络丛上皮细胞的纤毛发生与维持。正是这种Ca²⁺稳态失衡,最终导致脑脊液稳态失衡和脑积水的发生。
该研究首次揭示了Piezo1介导的机械转导在脉络丛上皮细胞纤毛稳态和脑脊液动力学中的关键作用,为理解交通性脑积水的发生机制提供了新的分子机制。研究同时强调针对Piezo1相关通路的干预不能简单理解为“激活”或“抑制”,而更应着眼于恢复机械转导与Ca²⁺信号的稳态窗口。这一点对于未来探索脑积水及其他脑脊液动力学异常疾病的精准干预策略具有重要启发意义。
综上,研究建立了一个由Piezo1主导的脉络丛机械转导新机制:机械刺激通过机械力受体Piezo1调控脉络丛上皮细胞Ca²⁺稳态,进而维持脉络丛上皮细胞纤毛发生和脑脊液稳态;当这一系统发生双向失衡时,诱发脑积水。该工作不仅拓展了对脉络丛神经生物学功能的认识,也为脑积水等机械力相关性脑室系统疾病提供了新的病理机制启示与潜在干预靶点。
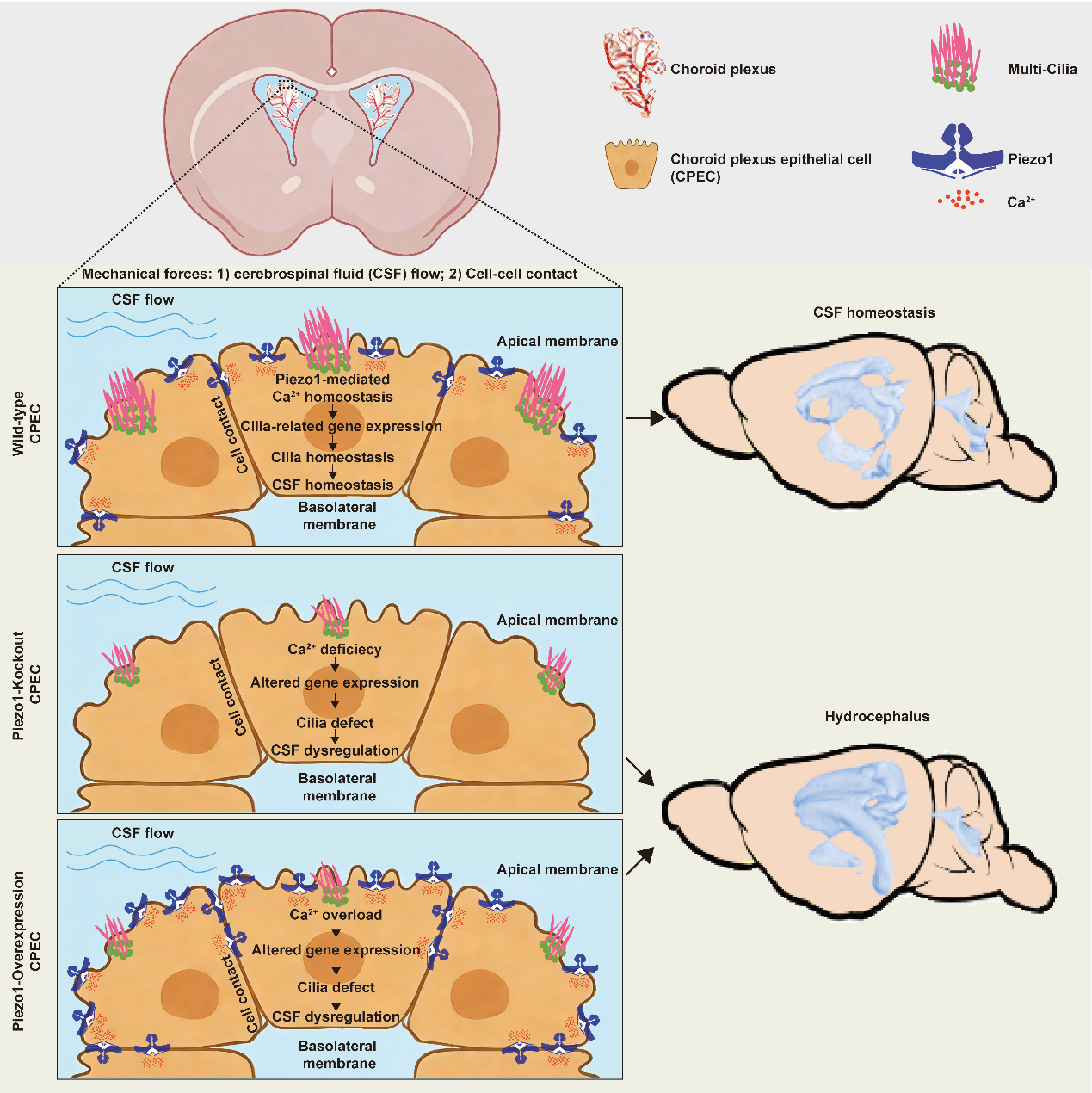
Piezo1介导脉络丛上皮细胞的机械信号转导、纤毛发生与脑脊液稳态维持
研究成果以“Piezo1所介导的脉络丛上皮细胞机械信号转导调控纤毛发生以及脑脊液稳态维持”(Piezo1-mediated mechanotransduction in choroid plexus epithelial cells governs ciliogenesis and cerebrospinal fluid homeostasis)为题,于3月30日发表于《神经元》(Neuron)。
清华大学药学院教授肖百龙为论文通讯作者,药学院已毕业博士生朱肖与2024级博士生朱佳杰为论文共同第一作者。
研究得到国家自然科学基金重点项目/创新研究群体项目、科技创新2030—“脑科学与类脑研究重大项目”、新基石研究员项目、北京市卓越学者项目、教育部基础与交叉学科突破计划等的资助,同时得到清华-北大生命科学联合中心、北京市生物结构前沿研究中心、膜生物学全国重点实验室和清华-IDG/麦戈文脑科学研究院的支持。
论文链接:
https://www.sciencedirect.com/science/article/pii/S0896627326001388?sessionid=
供稿:药学院
编辑:李华山
审核:郭玲