清华新闻网2月24日电 核心菌种是生物制造产业的“芯片”,决定了发酵工艺的效率、成本与产品竞争力。当前,我国生物制造产业的核心菌种超过80%依赖进口,从大宗氨基酸、有机酸到酶制剂,诸多关键生产菌株依赖国外。这一局面不仅推高了技术引进与工艺适配的成本,更在产业链供应链层面埋下隐患。在生物经济上升为国家战略、新型工业化加速推进的背景下,核心微生物菌种的自主可控已成为行业必须突破的瓶颈。
清华大学生命学院陈国强教授团队从野生环境中分离得到耐盐碱的嗜盐菌(Halomonasspp.)天然菌株,开展了二十年余年系统攻关,成功创制出具有完全自主知识产权的新型底盘细胞——Halomonas bluephagenesis TD系列及其衍生菌株,实现在开放条件下连续发酵,彻底规避灭菌环节,显著降低能耗与设备成本,在国际上首次提出并建立了基于极端微生物的下一代工业生物技术(NGIB)。然而,嗜盐菌底盘依赖较高盐度(通常30-60g/L NaCl)以维持细胞生理稳态与代谢活性。这一高盐依赖在一定程度上限制了其在更低盐、更灵活工艺体系中的应用拓展,也增加了后续废水处理与环境负荷。如何在保持开放非无菌培养优势的同时,降低嗜盐菌对高盐环境的依赖,从而构建更节能、更低碳、更普适的国产自主生物制造平台,是该领域亟须突破的关键科学问题。
针对上述挑战,陈国强团队采用迭代工程化改造策略,系统优化菌株的低盐适应性,成功构建了在仅含0.1%(w/v)NaCl条件下仍可稳健生长的SSM系列工程菌株。该研究围绕该系列菌株的构建逻辑、低盐适应机制及其生物合成性能展开系统阐述,为嗜盐菌底盘的精细化工程改造提供新范式,也为我国自主知识产权工业菌株的深度优化与产业化应用奠定理论依据与技术储备。
2月11日,研究成果以“工程化改造盐单胞菌实现低盐条件下的开放式非无菌聚羟基丁酸合成”(EngineeringHalomonasfor Low Salt Open Unsterile Production of Polyhydroxybutyrate)为题,在线发表于《生物技术趋势》(Trends in Biotechnology)。研究以嗜盐菌Halomonas bluephagenesis为研究对象,通过系统性的工程化改造,构建了一系列在低盐条件下仍保持稳健生长能力的工程化菌株。采用迭代式“优中选优”的工程策略,研究团队在逐轮筛选与优化中获得了高度适应低盐环境的H.bluephagenesis TD 1.0 SSM系列菌株。该系列菌株在盐度最低仅0.1%(w/v)NaCl且pH=9的高碱性条件下仍可稳定生长,同时保留其在高盐环境中的耐受特性,从而显著拓展了嗜盐菌的渗透压适应范围。
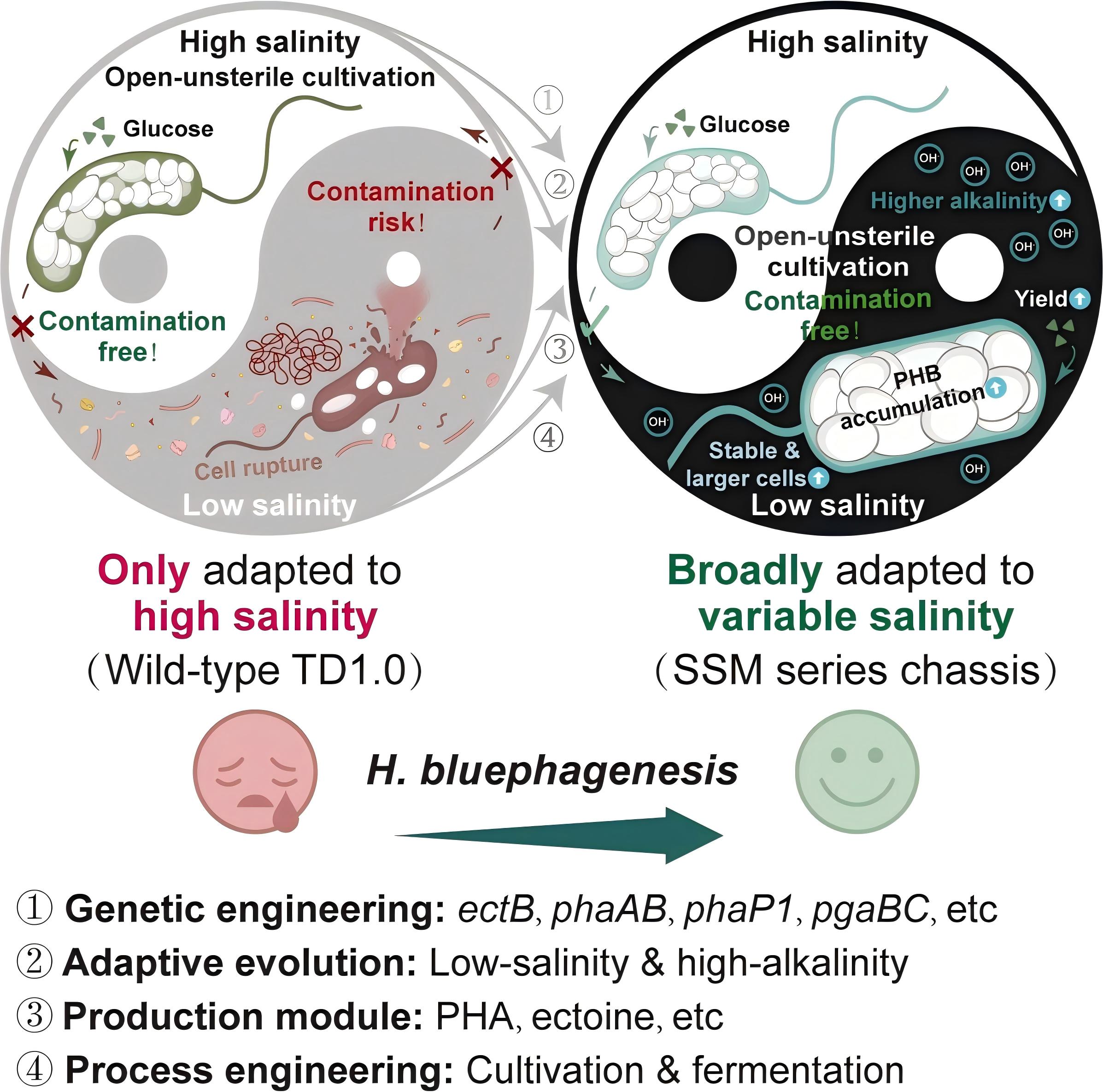
图1.图形摘要
研究团队综合运用了基因编辑、适应性实验室进化、代谢重构以及发酵过程工程等多种策略,对H.bluephagenesis的渗透压调控、细胞形态与代谢网络进行了系统优化。多组学与表型分析结果显示,低盐适应型菌株在细胞表面性质、细胞形态及群体行为等方面发生了显著改变,表现为细胞体积增大、自发絮凝增强以及生物合成能力的整体提升。在7L生物反应器中,该工程菌株在仅含有5g/L NaCl的矿物培养基发酵条件下即可实现稳定的开放非无菌培养,并在44小时内获得最高约76g/L的细胞干重,其中PHB含量高达86%,碳源底物葡萄糖到PHB的转化率约39%。上述结果表明,该工程化嗜盐菌体系在显著降低盐度依赖的同时,仍可保持优异且稳定的生物制造性能,不仅为未来节能、低碳、低成本的工业生物技术路线提供了可行范式,也拓展了嗜盐菌在更广泛工艺条件下的应用潜力。此外,研究系统揭示了嗜盐菌在低渗环境下的适应性重构特征,为深入理解微生物渗透压适应与环境响应机制提供了重要实验基础和新的研究证据。
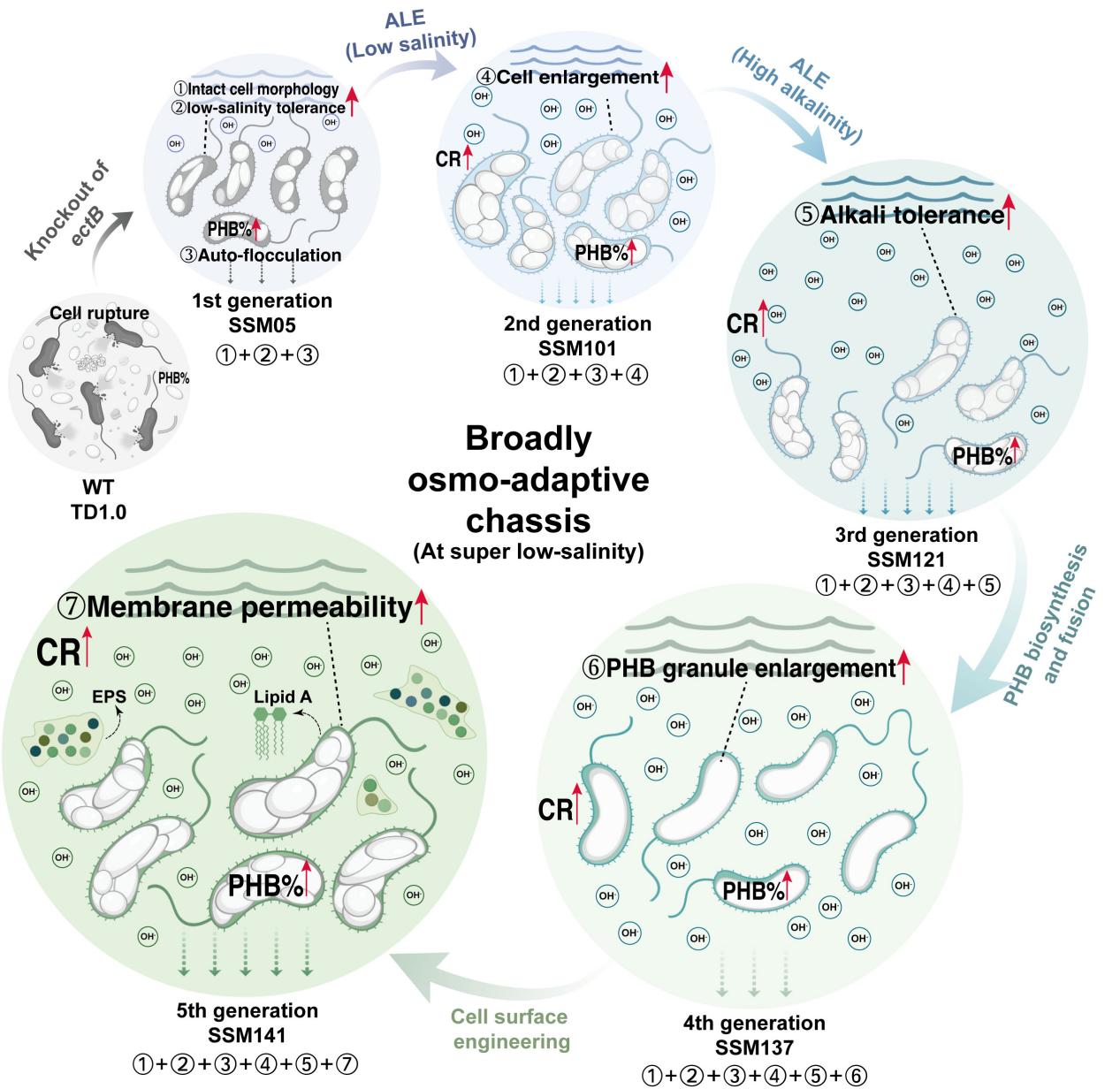
图2.迭代工程化改造构建的广域盐度适应型H.bluephagenesis SSM系列底盘的模式图
清华大学生命学院教授陈国强为论文通讯作者,生命学院2021级博士生孙思勉为论文第一作者,生命学院2022级博士生邵明威、2024届博士毕业生胡启跳、2025届博士毕业生金云帆、2024届博士毕业生张忠楠为研究作出重要贡献,生命学院副研究员吴赴清参与了课题指导与帮助。研究得到科技部国家重点研发计划和国家自然科学基金的资助,同时得到北京微构工厂、清华-北大生命科学联合中心以及清华大学生物医学分析中心下属电镜平台的大力支持。
论文链接:
https://doi.org/10.1016/j.tibtech.2026.01.002
供稿:生命学院
编辑:李华山
审核:郭玲