清华新闻网2月15日电 压电材料凭借机械信号与电信号的双向转换特性,在生物医用领域展现出广阔应用前景,目前已逐步应用于组织再生、生物传感等领域。但现有的压电器件多采用不可降解材料,术后需通过二次手术取出,易引发组织损伤与感染风险;传统可降解压电材料普遍存在压电性能弱、柔韧性与压电性不兼容等问题,兼具高压电性能与可降解性的材料研发仍是行业关键挑战。
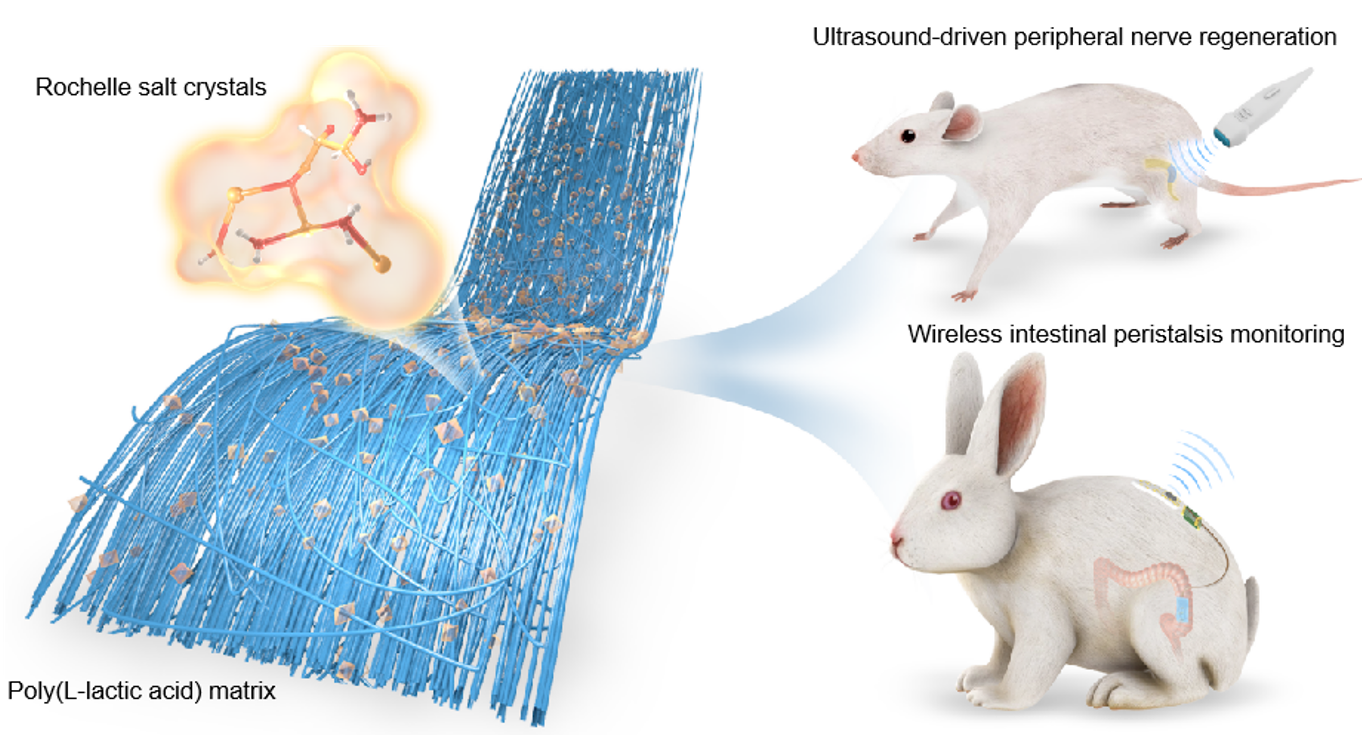
图1. 罗谢尔盐基可降解压电复合材料及其生物应用示意图
近日,清华大学材料学院尹斓副教授团队联合中国人民解放军总医院骨科医学部研究所彭江所长、王玉研究员团队,中国人民解放军总医院神经外科医学部张军主任团队,中国人民解放军总医院第九医学中心田磊主任团队,研发出基于罗谢尔盐的可降解柔性压电复合材料及器件,并实现了其在生物医学领域的应用。该材料兼具优异的压电性能、生物相容性与生物可降解性,实现了超声驱动的周围神经再生和肠道蠕动的无线实时监测,为再生医学与生理监测领域提供了全新的材料与技术范式。
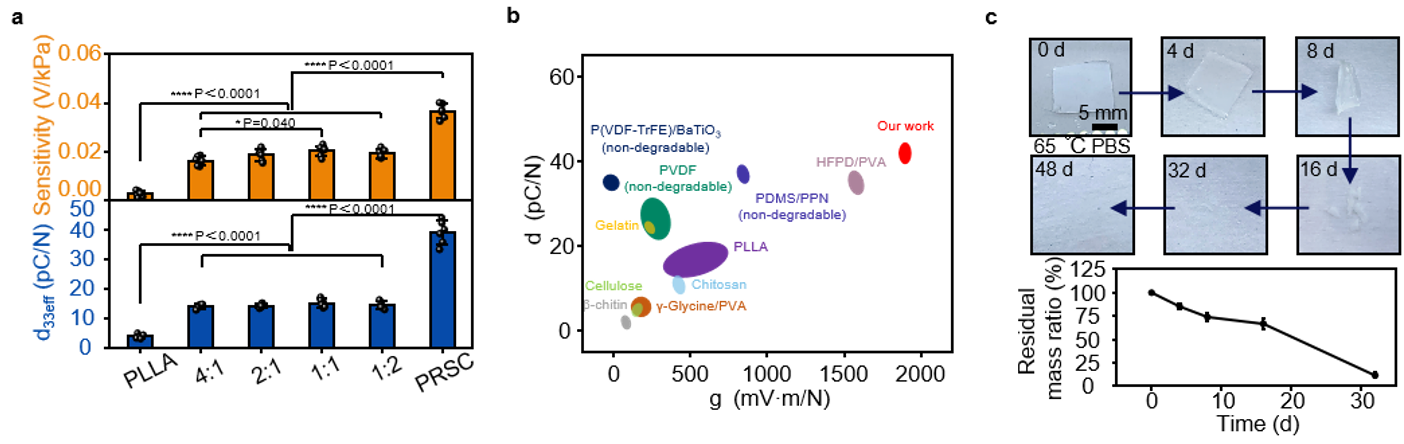
图2.罗谢尔盐基可降解压电复合材料的压电性能与可降解性
研究团队以具有生物相容性的罗谢尔盐为压电核心,与左旋聚乳酸(PLLA)复合,通过静电纺丝结合单轴压缩的创新工艺,制备出可降解压电复合材料。该材料突破了传统可降解压电材料的性能瓶颈,有效压电系数d33eff达43.1 pC N-1,较纯聚乳酸纤维提升超10倍,压电电压系数达1909.2 mV m N-1,综合性能超越现有多数可降解材料,甚至部分非降解压电材料;同时兼具良好的柔韧性与生物相容性,可在生理环境中逐步降解,无需二次手术取出。基于此,研究团队进一步开发了超声响应型压电神经支架和可降解压电应变传感器。前者成功实现了大鼠10mm坐骨神经缺损再生和运动功能恢复,有效缓解肌肉萎缩;后者可有效捕捉新西兰白兔肠道蠕动幅度、波速、频率等关键参数,实现药物干预后肠道动力变化及急性肠系膜缺血的早期检测。
研究成果以“用于神经再生和肠道蠕动监测的罗谢尔盐基可生物降解压电器件”(Rochelle salt-based biodegradable piezoelectric devices for nerve regeneration and intestinal motility monitoring)为题,于1月29日在线发表于《自然·通讯》(Nature Communications)。
清华大学材料学院2025届博士毕业生戴凡淇,南开大学2024级博士生程浩峰,北京市创伤骨科研究所綦惠副研究员为论文共同第一作者,尹斓、王玉、张军和田磊为论文共同通讯作者。清华大学电子系张沕琳副教授团队,马骋副教授团队和盛兴副教授团队也参与了工作。研究得到国家自然科学基金、北京市自然科学基金和清华-丰田联合研究基金等的支持。
论文链接:
https://www.nature.com/articles/s41467-026-68930-2
供稿:材料学院
编辑:杨雪文
审核:周襄楠