清华新闻网10月10日电 真核生物染色质中,组蛋白末端的共价翻译后修饰(如乙酰化、甲基化、泛素化等)对调控基因转录、DNA复制等过程具有重要作用。其中,组蛋白乙酰化与组蛋白H3K4me3修饰常与基因活跃转录相关,而H3K27me3修饰则发挥转录抑制作用。前期研究发现,拟南芥中存在兼具组蛋白乙酰化和H2A去泛素化功能的PEAT复合体,其与基因转录激活密切相关,且包含功能冗余的DNA结合蛋白TRB1和TRB2。此外,TRB蛋白可结合H3K4me3去甲基化酶JMJ14,以及负责H3K27me3修饰的PRC2复合体组分。然而,TRB蛋白如何整合不同复合体功能,在全基因组层面协调不同组蛋白修饰,是领域内尚待解决的关键科学问题。
北京时间10月6日,北京生命科学研究所/清华大学生物医学交叉研究院何新建实验室在《先进科学》(Advanced Science)在线发表了题为“拟南芥TRB蛋白形成两个密切相关的复合物介导H3K4me3去甲基化和转录抑制”(Arabidopsis TRB proteins form two closely related complexes to mediate H3K4me3 demethylation and transcriptional repression)的研究论文。该研究发现了拟南芥中两种紧密关联的新型复合体TRHT和TRHD,揭示了它们协同其他组蛋白修饰介导组蛋白H3K4me3去甲基化的分子机制。
该研究通过蛋白亲和纯化结合质谱分析(AP-MS)系统鉴定出TRB1、TRB2、TRB3(TRB1/2/3)的结合蛋白,证实TRB1/2/3不仅参与PEAT复合体和PRC2复合体的形成,还能组装成两种功能冗余的新型复合体:TRHT(包含TRB1/2/3、ICU11和HTH1/2/3)与TRHD(包含TRB1/2/3、ICU11、JMJ14、NAC050/052和ZDP2),其中TRB1/2/3和ICU11是这两个复合体的共有亚基(图1A)。随后,研究利用酵母双杂交、体外pull-down等实验,进一步明确了两个复合体各组分之间的相互作用模式(图1B)。

图1.TRHT/TRHD复合体组分间结合方式
为探究TRHT/TRHD复合体在全基因组水平的作用,该研究通过染色质免疫沉淀测序(ChIP-seq),比较了TRHT、TRHD、PEAT和PRC2这几类包含TRB蛋白的复合体在全基因组的分布。结果显示,尽管TRHT和TRHD具有特异亚基,但是二者在全基因组水平共同占据大量靶基因,且其分布与PEAT、PRC2复合体显著不同,凸显TRHT/TRHD复合体的独特性。进一步分析发现,TRHT/TRHD与PEAT的靶基因重叠水平较高,共享大量共同靶基因,而与PRC2的靶基因重叠水平较低(图2)。
在功能机制上,研究发现TRHT/TRHD 靶基因呈中等水平的H3K4me3修饰,介于具有高水平H3K4me3修饰的PEAT靶基因与低水平H3K4me3修饰的PRC2靶基因之间。TRHT/TRHD可通过JMJ14介导的H3K4me3去甲基化抑制基因表达,且这种调控具有染色质环境依赖性。当靶基因同时被PRC2识别时,H3K4me3去甲基化作用显著增强;而在与PEAT共享的靶基因中,该作用则被抑制,表明TRHT/TRHD的H3K4me3去甲基化功能受所在区域其他组蛋白修饰的动态调控。

图2.TRHT/TRHD复合体组分在靶基因上的富集信号
研究进一步结合ChIP-seq、电泳迁移率变动分析(EMSA)和等温滴定量热法(ITC)等多种实验,揭示了TRHT/TRHD结合基因组上特定靶位点的分子机制。TRB蛋白通过N端的Myb结构域识别特定的DNA基序,NAC050/052作为转录抑制因子结合另一类DNA基序,二者协同作用增强复合体与靶位点的结合能力;HTH1则以非序列依赖的方式辅助结合DNA,确保复合体与靶位点结合的高效性(图3)。此外,TRB1的Myb结构域对复合体的生物学功能至关重要,缺失后会令拟南芥出现严重发育缺陷,证实其是维持复合体功能的核心元件。
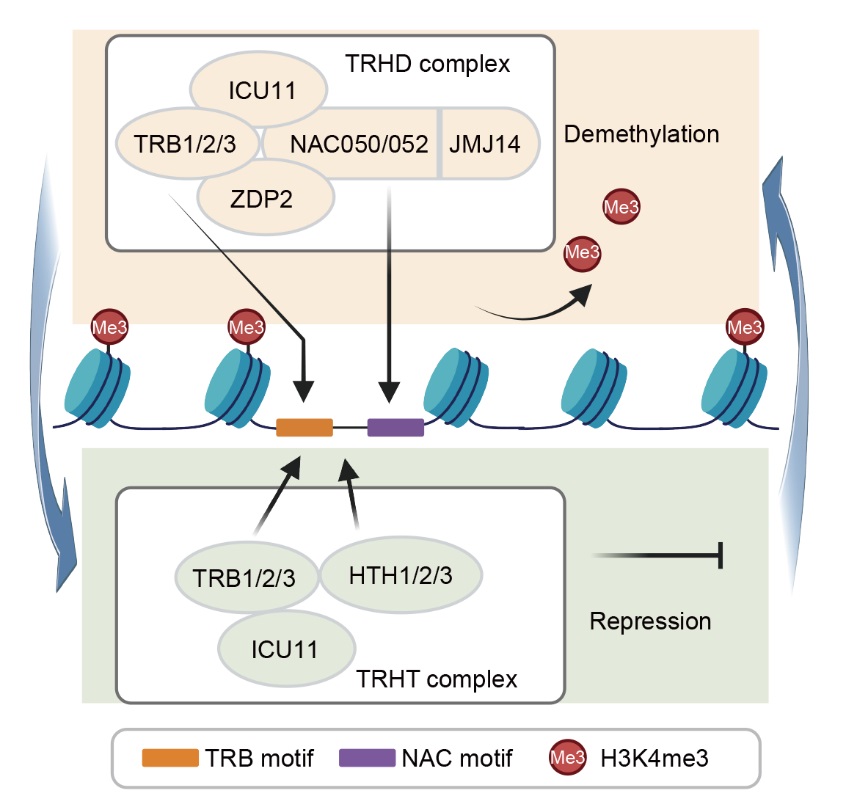
图3.TRHT/TRHD复合体工作模式图
综上,研究发现TRB家族蛋白所形成的两种新型蛋白复合体,阐明了它们与PEAT、PRC2复合体协同作用模式,揭示了植物对多种染色质修饰的协同调控机制,为理解植物复杂性状的表观遗传调控提供了全新视角。
北京生命科学研究所/清华大学生物医学交叉研究院何新建实验室2021级博士生王琪为论文第一作者,何新建研究员为论文通讯作者。研究得到科技部和国家自然科学基金委的资助。
论文链接:
http://doi.org/10.1002/advs.202503420
供稿:生物医学交叉研究院
编辑:李华山
审核:郭玲